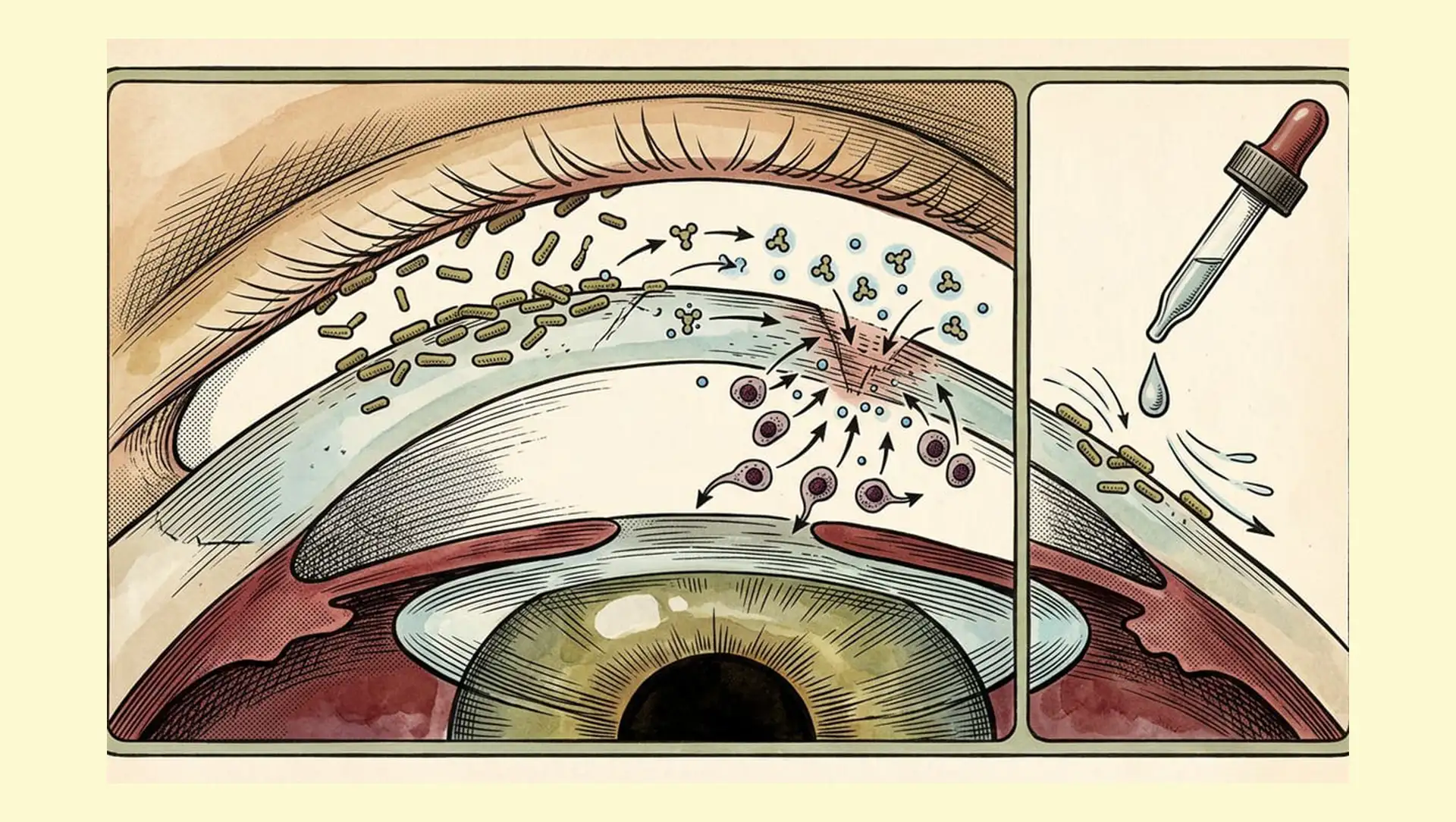
Die Idee klingt zunächst ungewöhnlich, könnte aber die Behandlung von Erkrankungen der Augenoberfläche grundlegend verändern: Statt klassischer Augentropfen setzen Forschende auf lebende Mikroorganismen, die therapeutische Wirkstoffe direkt am Auge produzieren. Ein Team der University of Pittsburgh hat nun gezeigt, dass sich natürliche Augenbakterien gentechnisch so verändern lassen, dass sie entzündungshemmende Substanzen freisetzen und so die Heilung der Hornhaut beschleunigen.
Warum klassische Augentropfen an ihre Grenzen stoßen
Erkrankungen der Hornhaut und Augenoberfläche gelten als therapeutisch herausfordernd. Ein zentrales Problem besteht darin, dass topisch applizierte (also lokal angewendete) Medikamente durch den Tränenfilm rasch verdünnt und ausgeschwemmt werden. Die Folge ist ein hoher Applikationsaufwand mit mehrfach täglicher Anwendung, was die Therapietreue deutlich beeinträchtigen kann.
Gerade bei chronischen Erkrankungen wie dem Trockenen Auge oder bei wiederkehrenden Hornhauterosionen gilt dies als limitierender Faktor. Vor diesem Hintergrund erscheint der Ansatz einer dauerhaft wirksamen, sich selbst erhaltenden Therapie besonders attraktiv.
Gentechnisch veränderte Augenbakterien als Wirkstoffproduzenten
Im Mittelpunkt der aktuellen Studie, erschienen in der Fachzeitschrift Cell Reports, steht das Bakterium Corynebacterium mastitidis. Es kommt natürlicherweise auf der Augenoberfläche vor und gilt als apathogen, verursacht also unter normalen Bedingungen keine Erkrankungen.
Den Forschenden zufolge wurde der Mikroorganismus genetisch so modifiziert, dass er kontinuierlich Interleukin 10 freisetzt – ein Zytokin, also ein kleines Signalprotein des Immunsystems mit entzündungshemmender und immunregulierender Wirkung.
Der leitende Autor, Anthony St. Leger vom UPMC Vision Institute, spricht vom ersten Nachweis, dass ein natürlicher Mikroorganismus auf der Augenoberfläche gezielt so verändert werden kann, dass er ein therapeutisch wirksames Molekül produziert und damit die Augengesundheit verbessert. Dieser Ansatz öffne die Tür zu einer Art „lebender Medizin“, die nach einmaliger Anwendung langfristig am Wirkort verbleiben könnte.
Beschleunigte Hornhautheilung: Was zeigen aktuelle Versuche über den neuen Therapieansatz?
Bei Tierversuchen im Mausmodell zeigte sich ein deutlicher Effekt: Tiere mit Hornhautverletzungen, die mit den veränderten Bakterien behandelt wurden, wiesen eine schnellere Heilung des Hornhautepithels auf als Vergleichsgruppen. Wurde der Rezeptor für Interleukin 10 blockiert, verschwand dieser Vorteil – ein Hinweis auf die zentrale Rolle des Zytokins.
Darüber hinaus entwickelten die Forschenden eine Variante des Bakteriums, die humanes Interleukin 10 produziert. In Zellkulturversuchen mit menschlichen Hornhautepithelzellen führte dies zu einem verbesserten Wundverschluss. Gleichzeitig wurden entzündungsfördernde Signalwege in Immunzellen reduziert – ein zusätzlicher Hinweis auf die potenzielle Übertragbarkeit auf den Menschen.
Modulares Therapiekonzept: Kann eine bakterielle Therapie individuell angepasst werden?
Besonders interessant erscheint der modulare Aufbau des Systems. Laut St. Leger lässt sich die Plattform so anpassen, dass unterschiedliche therapeutische Proteine produziert werden – etwa regenerative oder entzündungshemmende Substanzen. Damit könnte die Technologie langfristig für verschiedene Erkrankungen der Augenoberfläche nutzbar sein.
In der Forschung wird dieser Ansatz als „lebendes Biotherapeutikum“ bezeichnet – eine Therapieform, bei der lebende Mikroorganismen gezielt zur Wirkstoffproduktion eingesetzt werden. Vergleichbare Strategien werden bereits für Darmerkrankungen untersucht.
Sicherheitsfragen & Entwicklungsbedarf: Wie sicher ist die Anwendung lebender Augentropfen wirklich?
Trotz der vielversprechenden Ergebnisse handelt es sich bislang um eine frühe Proof-of-Concept-Studie. Vor einer klinischen Anwendung sind zahlreiche Hürden zu überwinden, betonen die Autoren der Studie. Dazu zählt insbesondere die Entwicklung sogenannter Kill-Switch-Mechanismen, mit denen sich die modifizierten Bakterien bei Bedarf gezielt inaktivieren oder eliminieren lassen.
Auch Fragen der Langzeitsicherheit und regulatorische Anforderungen werden entscheidend sein, falls der Ansatz in Richtung klinischer Studien weiterentwickelt wird.
Vision einer selbstregulierenden Therapie
Für die augenoptische Praxis ergibt sich zunächst noch keine unmittelbare Anwendung. Perspektivisch könnte die Technologie jedoch Einfluss auf die Therapie chronischer Erkrankungen der Augenoberfläche nehmen, die auch im optischen Alltag häufig vorkommen.
Gerade bei Betroffenen mit Trockenen Augen oder nach Hornhautverletzungen könnte eine langfristig wirksame, selbstregulierende Therapie die Abhängigkeit von häufig applizierten Augentropfen verringern. Das würde nicht nur die Compliance (also die Bereitschaft eines Patienten zur aktiven Mitwirkung an therapeutischen Maßnahmen) verbessern, sondern möglicherweise auch zu einer nachhaltigeren Versorgung beitragen.
Der Einsatz gentechnisch veränderter Augenbakterien markiert einen innovativen und zugleich wissenschaftlich plausiblen Ansatz in der Ophthalmologie. Die vorliegenden Daten deuten darauf hin, dass lebende Mikroorganismen künftig als kontinuierliche Wirkstoffquelle auf der Augenoberfläche dienen könnten. Bis zur klinischen Anwendung ist es zwar noch ein weiter Weg – doch die Studie liefert eine solide Grundlage für die Entwicklung einer Therapie, die das Prinzip der herkömmlichen Augentropfen grundlegend in Frage stellen könnte.
Studie: Jackie Shane, Matthew Evans, Yannis Rigas, Robert M.Q. Shanks, Anthony J. St. Leger. Genetically engineered eye-colonizing microbes that deliver the anti-inflammatory cytokine interleukin-10 enhance corneal tissue repair. Cell Reports2026.